
概要:化学是一个很有趣的课程,想学好化学只是认真听课是不够的,还需要多做实际操作,一边实验一边思考,在实验中理解所学知识,发现新知识。本文为大家总结了高二化学中几种重要的金属的知识点供大家参考。一、金属1、金属的通性:一般为不透明、有金属光泽的固体,有良好的延展性、导电性和导热性。2、合金:一般来说,合金的熔点比各成分金属的都低,硬度比各成分金属的都大。3、金属的冶炼:冶炼步骤:富集→还原→精炼 冶炼方法:K、Ca、Na、Mg、Al(电解法),Zn、Fe、Sn、Pb、Cu(热还原法),Hg、Ag(热分解法)等。二、镁及其化合物1、镁的主要用途是制造各种轻合金(用于飞机、汽车等)。2、重要方程式:Mg+O2 = 2MgO Mg+2H2O=Mg(OH)2+2H2↑ 2Mg+CO2=2MgO+CMgO+H2O=Mg(OH)2 MgCO3=MgO+CO2↑(煅烧菱镁矿制MgO) MgCl2(熔融) = Mg+Cl2↑三、铝及其化合物1、铝的重要反应:4Al+3O2=2Al2O3 2Al+3S=Al2S3 2Al+6H2O=2Al(
高二化学知识点总结:几种重要的金属,标签:高二语文知识点梳理大全,高二学习方法,http://www.kgf8.com化学是一个很有趣的课程,想学好化学只是认真听课是不够的,还需要多做实际操作,一边实验一边思考,在实验中理解所学知识,发现新知识。本文为大家总结了高二化学中几种重要的金属的知识点供大家参考。
一、金属
1、金属的通性:一般为不透明、有金属光泽的固体,有良好的延展性、导电性和导热性。
2、合金:一般来说,合金的熔点比各成分金属的都低,硬度比各成分金属的都大。
3、金属的冶炼:冶炼步骤:富集→还原→精炼 冶炼方法:K、Ca、Na、Mg、Al(电解法),Zn、Fe、Sn、Pb、Cu(热还原法),Hg、Ag(热分解法)等。
二、镁及其化合物
1、镁的主要用途是制造各种轻合金(用于飞机、汽车等)。
2、重要方程式:Mg+O2 = 2MgO Mg+2H2O=Mg(OH)2+2H2↑ 2Mg+CO2=2MgO+C
MgO+H2O=Mg(OH)2 MgCO3=MgO+CO2↑(煅烧菱镁矿制MgO) MgCl2(熔融) = Mg+Cl2↑
三、铝及其化合物
1、铝的重要反应:4Al+3O2=2Al2O3 2Al+3S=Al2S3 2Al+6H2O=2Al(OH)3+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑(重点反应) 2Al+6HCl=2AlCl3+3H2↑2Al+Fe2O3=Al2O3+2Fe(铝热反应,用于冶炼难熔金属和焊接钢轨) 2Al2O3(熔融)=2Al+3O2↑[工业炼铝]
2、Al2O3和Al(OH)3:中学化学唯一的两性氧化物和两性氢氧化物。
重要反应:Al2O3+6H+=2Al3++3H2O Al2O3+2OH-=2AlO2-+H20 Al(OH)3+3H+=Al3++2H2O
Al(OH)3+OH-=AlO2-+2H2O H++AlO2-+H2O Al(OH)3 Al3++3OH-(氢氧化铝的电离)
3、明矾:KAl(SO4)2•12H2O,是一种复盐,作净水剂(简单解释原因)。明矾与Ba(OH)2反应
(难点):当Al3+恰好完全沉淀时:2KAl(SO4)2 + 3Ba(OH)2=2Al(OH)3↓+3BaSO4↓+K2SO4,
当SO42-恰好完全沉淀时:KAl(SO4)2 + 2Ba(OH)2= =KAlO2+2BaSO4↓+2H2O。
4、氢氧化铝的制备:可以用铝盐与过量氨水(强碱不好因不易控制用量)或铝盐与偏铝酸盐双水解或偏铝酸盐与过量的CO2反应。Al3++3NH3•H2O=Al(OH)3↓+3NH4+ ,
Al3++3AlO2-+6H2O=4Al(OH)3↓,AlO2-+CO2+H2O=HCO3-+Al(OH)3↓
5、有关Al3+与OH-反应的图象、互滴及计算:要会画两种情况的图象,知道互滴现象,会进行有关计算(计算时需要讨论Al3+与OH-谁过量)。(计算中如果有Mg2+,要注意使用守恒法。)
四、铁及其化合物
1、铁的位置:原子序数为26,位于第四周期Ⅷ族,属过渡元素,原子结构示意图为:
2、铁的氧化物及氢氧化物的对比(见参考书绿色通道),注意:氧化铁—红棕色,Fe3O4中Fe的化合价,Fe(OH)3—红褐色 Fe(OH)2的制备—胶头滴管违反常规操作的原因(?)等
3、重要反应:3Fe+2O2=Fe3O4 3Fe+4H2O(g)=Fe3O4+4H2 2Fe+3Cl2=2FeCl3(棕黄色烟) 2Fe3++Fe=3Fe2+ Fe2++2OH_=Fe(OH)2↓ 4Fe(OH)2+O2+2H2O=4Fe(OH)3(白色沉淀迅速变成灰绿色,最终变成红褐色) Fe(OH)3=Fe2O3+3H2O Fe3++3SCN_=Fe(SCN)3[溶液变红色,检验Fe3+]
4、重要补充反应:2Fe3++Cu=2Fe2++Cu2+ 2Fe2++Cl2=2Fe3++2Cl_ 2Fe3++H2S=2Fe2++S↓+2H+
Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O(铁不足) 3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O(铁过量)
5、其他问题:包括计算(注意差量法和守恒法)、氧化还原反应的先后顺序问题、Fe2+的保存(防止水解及被氧化的措施:加少量稀酸和铁粉)等。重点提示:铁的转化最容易出现在推断题中,以Fe2O3的红棕色及Fe(OH)2→Fe(OH)3的明显现象作为突破口,有时会牵涉到铝热反应以及铁与盐酸、氯气反应分别生成FeCl2、FeCl3等知识点。
www.kgf8.com
五、原电池的化学原理
1.原电池是将化学能转化为电能的装置。
2.电子流出的一极是负极,通常是活泼性较强的金属,电极被氧化,发生氧化反应。
电子流人的一极是正极,通常是活泼性较弱的金属或非金属导体,电极上发生还原反应。
如 铜—锌原电池 (电解液是稀硫酸) 负极(锌片):Zn - 2e- = Zn2+(氧化反应)
正极(铜片):2H++ 2e- = H2↑(还原反应)
3.原电池中电子从负极流出,流入正极,与电流方向相反。
六、常见化学电源:
七、金属的电化学腐蚀
1、化学腐蚀与电化学腐蚀的比较
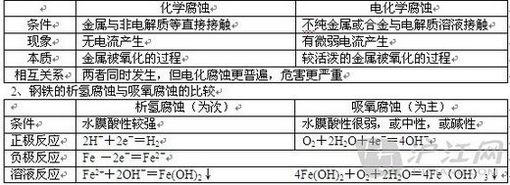
3、防止金属被腐蚀的方法:
(1)加保护层(表面涂油脂、喷漆、复盖搪瓷、电镀、喷镀、表面钝化等)。
(2)改变金属内部结构(制成不锈钢,如镍铬钢)。
(3)电化学保护法,如牺牲阳极法(在海轮船体吃水线下装上一定数量的锌块,防止船壳被腐蚀)。
 上一篇:高二上半年数学十五个重要知识点结
上一篇:高二上半年数学十五个重要知识点结
 保存 |
保存 |
 打印 |
打印 |
 关闭
关闭